Science China Life Sciences:张永清团队建立了基于载脂蛋白 E 缺失的动脉粥样硬化及临床并发症的家犬模型
2021年9月,中科院遗传发育所等单位的相关研究人员在《Science China-Life Sciences》(IF: 6.0)上发表了题为“Dogs lacking Apolipoprotein E show advanced atherosclerosis leading to apparent clinical complications”的研究论文,揭示了可用于动脉粥样硬化和脑中风等相关疾病的基础和转化研究的ApoE突变家犬模型。

ApoE KO 家犬表现出高胆固醇血症和严重的动脉粥样硬化,其特征是动脉狭窄和闭塞,以及中风和坏疽的临床表现。
F0 突变体中观察到的动脉粥样硬化可以通过种系传播给下一代。ApoE KO 家犬的中风相关蛋白水平发生了改变。
动脉粥样硬化是一种进行性炎症性疾病,其特征是脂质在动脉壁中积聚并因此增厚,是世界死亡的主要原因。高胆固醇血症与动脉粥样硬化的程度和进展直接相关。载脂蛋白 E (ApoE) 突变的小鼠模型一直是最广泛使用的动脉粥样硬化模型,但很少有显示出导致缺血诱导临床症状的晚期动脉粥样硬化斑块,这限制了它们在转化研究中的使用。 ApoE 在胆固醇代谢中起关键作用。ApoE 的一个关键生理作用是它能够介导含 ApoE 的脂蛋白与低密度脂蛋白 (LDL) 受体的高亲和力结合,从而导致脂蛋白的摄取和降解以及脂蛋白胆固醇的使用。ApoE 敲除 (KO) 小鼠、大鼠、兔和猪的胆固醇水平升高,并在主动脉等大动脉中出现明显的动脉粥样硬化。然而,在这些 ApoE 突变体中很少报道与晚期动脉粥样硬化相关的临床表现。 家犬是研究人类疾病的理想模型,因为它们在解剖学和生理学方面与人类非常相似。 此外,由于 30,000 多年以来狗与人类的同居和共同进化,它们具有相似的饮食和日常生活模式,导致非传染性疾病的模式与人类相似。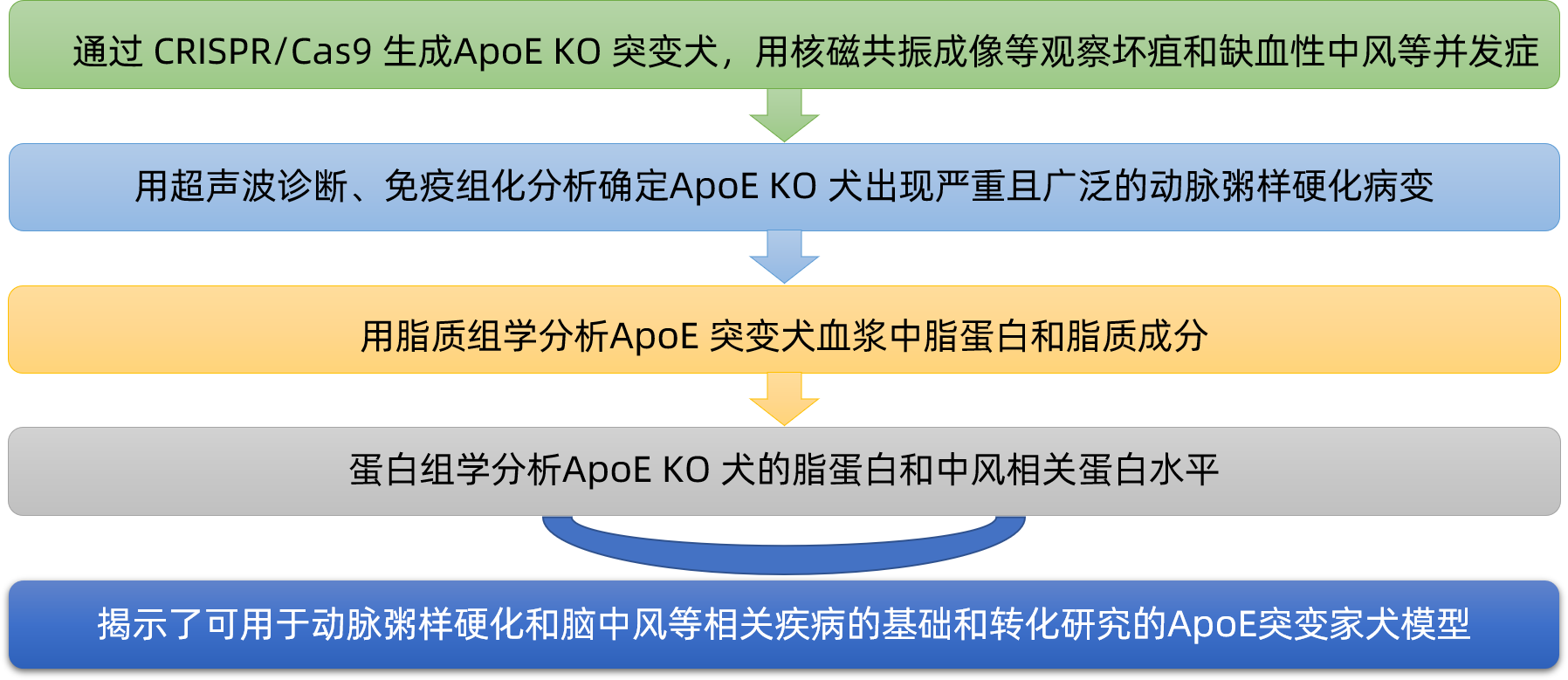
为了提供动脉粥样硬化的替代模型,研究人员之前通过 CRISPR/Cas9 生成了 ApoE KO 突变犬,然后使用体细胞核转移技术进行克隆。这些突变犬完全可以生育并且在18个月大的成年犬(12个月时性成熟)之前没有表现出任何明显的医学问题。然而在18-24个月大时出现了坏疽和缺血性中风等并发症,这个年龄相当于人类的40岁左右,与人类晚期动脉粥样硬化患者的病理相似。
接着,研究人员使用超声波诊断对四只 F0 成年 ApoE 突变犬进行了血管分析,并通过免疫组化分析检查了血管中的动脉粥样硬化迹象。结果发现,ApoE KO 犬在相应的动脉中出现严重且广泛的动脉粥样硬化病变。
此外,研究人员还发现,F0 突变体中观察到的动脉粥样硬化可以通过种系传播给下一代,F2 纯合 ApoE KO 犬重现了 F0 突变体的高胆固醇血症和动脉粥样硬化。研究人员通过脂质组学分析进一步分析了所有四只 F0 ApoE 突变犬血浆的脂质组成,发现主要脂质成分(例如胆固醇,但不是中链甘油三酯和磷脂酸)的水平显着上调,证实了 ApoE KO 突变体中的高胆固醇血症和正常的 TG 水平。
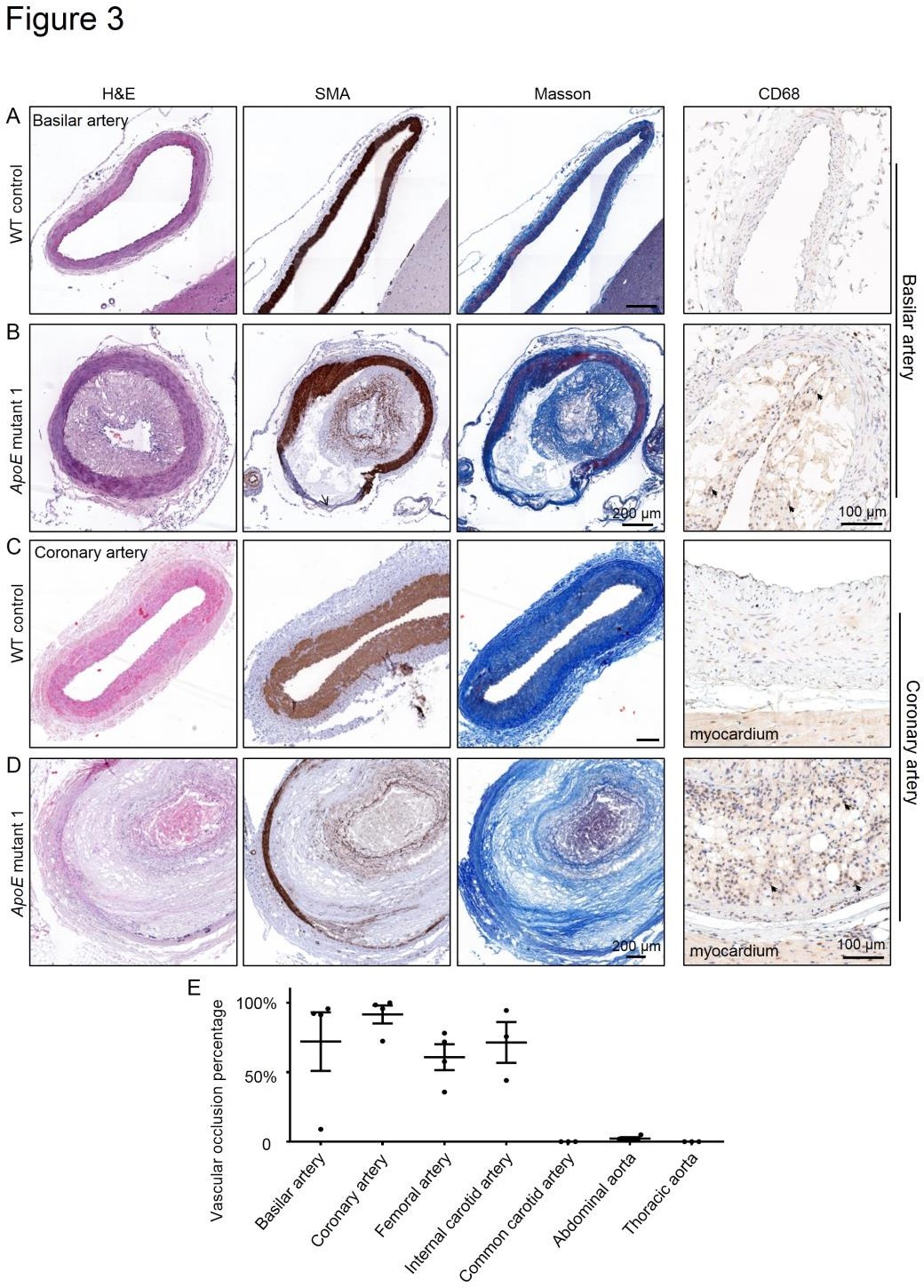
ApoE缺失突变体基底动脉和冠状动脉组织学染色显示严重动脉粥样硬化
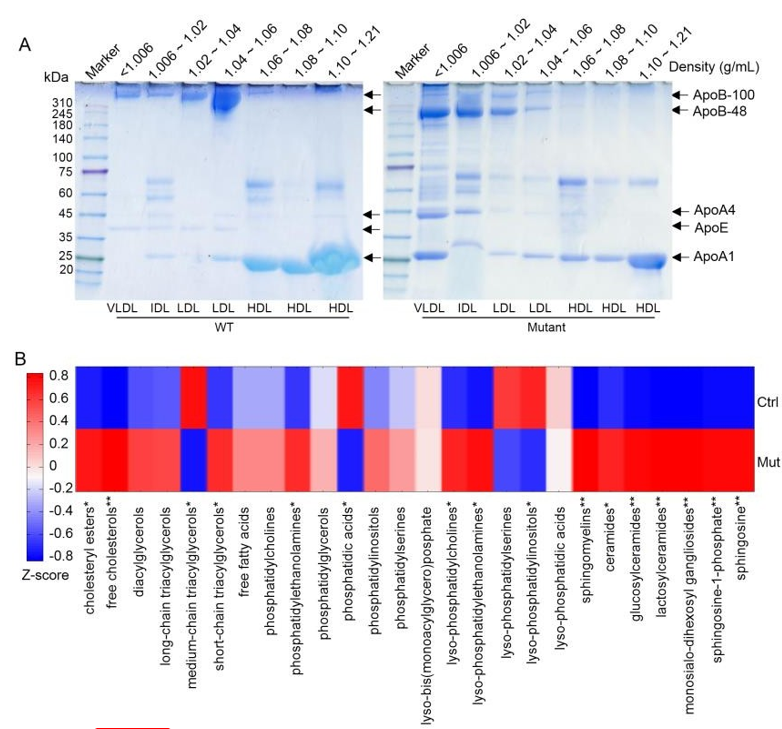
ApoE 突变犬血浆中脂蛋白和脂质成分的分析
最后,为了全面了解 ApoE 调控的分子途径,研究人员进行了蛋白质组学分析。对上调蛋白的功能富集分析表明,血浆和肝脏中共富集了六个过程,包括血液微粒、补体和凝血级联、细胞外空间和细胞外外泌体,而许多其他生物过程在血浆和肝脏这两个样本之间显示出不同的富集模式。且这些差异表达的蛋白质是与中风相关蛋白和全基因组关联研究 (GWAS) 阳性中风基因产物有所重叠。这些结果,尤其是肝脏蛋白质组学分析的结果,为 ApoE 及其相关通路在中风病因学中的关键作用提供了实验支持。
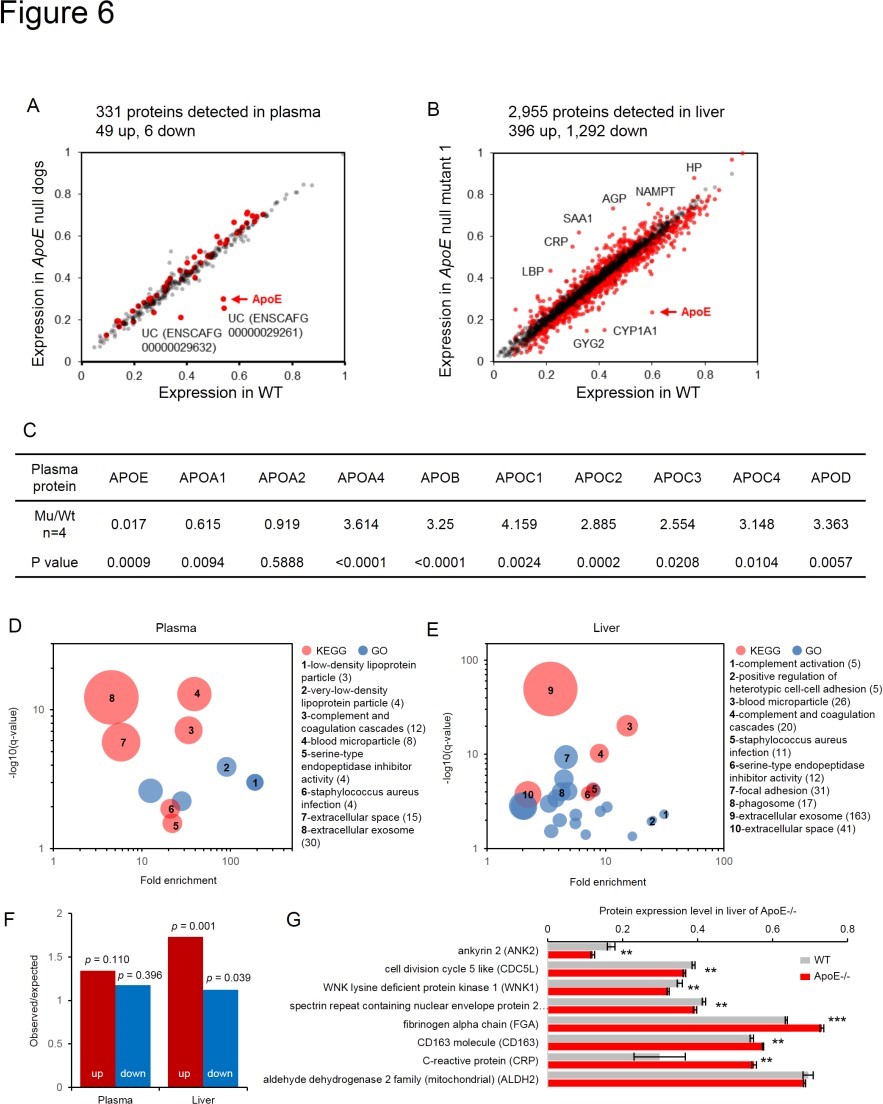
蛋白质组学分析显示 ApoE KO 犬的脂蛋白和中风相关蛋白水平发生了改变
综上所述,与其他动物模型相比, ApoE突变犬很好地重现了动脉粥样硬化病人的病理和临床表现。这些突变犬对于开发和评估新疗法(包括血管内手术)对抗动脉粥样硬化和相关疾病的新疗法将是非常宝贵的 。





