Nature Metabolism:GLP-1RA/tesaglitazar——降糖减重新分子
2022年8月,慕尼黑亥姆霍兹中心等单位的相关研究人员在《Nature Metabolism》(IF: 19.9)上发表了题为“GLP-1-mediated delivery of tesaglitazar improves obesity and glucose metabolism in male mice”的研究论文,报告了过氧化物酶体增殖物激活受体α和γ(PPARα/γ)双激动剂tesaglitazar与胰高血糖素样肽-1受体激动剂(GLP-1RA)共价连接的一种分子的临床前评估,揭示GLP-1RA/tesaglitazar可能对以高血糖和胰岛素抵抗为特征的疾病具有治疗价值。

亮点概述:
-
共价连接的胰高血糖素样肽-1受体激动剂(GLP-1RA)/tesaglitazar(过氧化物酶体增殖物激活受体α和γ(PPARα/γ)双激动剂)分子在体内外表现出GLP-1R依赖性PPARγ-9-顺式维甲酸受体(RXR)异源二聚化。
-
GLP1RA/tesaglitazar改善体重、食物摄入和葡萄糖代谢的疗效优于单独的GLP-1 RA或tesaglitazar。
-
GLP1RA/tesaglitazar增强的血糖作用可能是来自中枢神经系统,特别是下丘脑反馈的血糖调节器官介导的。
研究背景:
过氧化物酶体增殖物激活受体α和γ(PPARα/γ)在能量、脂质和葡萄糖代谢的调节中起重要作用。PPAR是一种核转录因子,在配体激活时与9-顺式维甲酸受体(RXR)异二聚化,通过与DNA反应元件结合促进靶基因表达。激活PPARα/γ的双激动剂(如tesaglitazar)对2型糖尿病患者的葡萄糖和脂质代谢有有益影响,但由于对心血管和/或肾脏系统的潜在不利影响,它们的开发已停止。
研究人员开发了一种经生物化学修饰的GLP-1RA肽,该肽可用于tesaglitazar的GLP-1R依赖性递送。在人胚胎肾293(HEK293)和源自转基因小鼠系胰岛素瘤的胰腺β细胞(MIN6细胞)中,研究人员发现,GLP-1RA/tesaglitazar在体外可促进GLP-1R介导的Gαs募集、cAMP生成,在内化和降解方面与药代动力学匹配的GLP-1RA具有相当的效力,该缀合物显示出GLP-1R依赖性PPARγ-RXR异源二聚化。
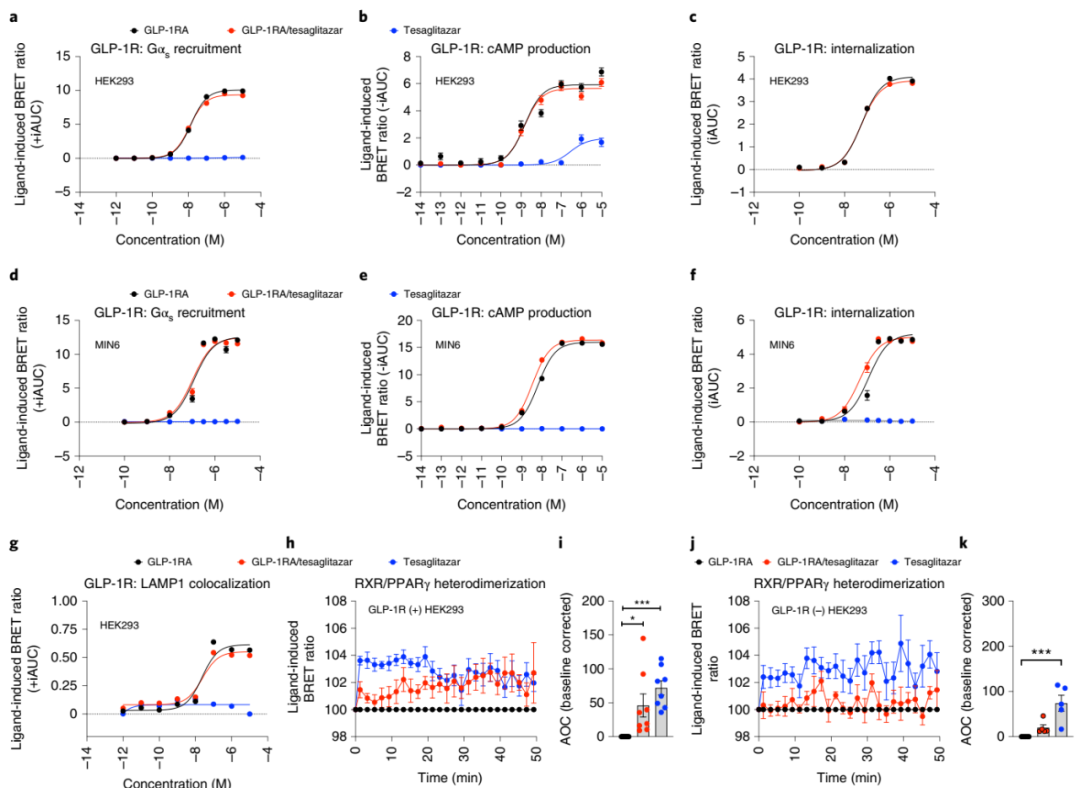
GLP-1RA/tesaglitazar 对 GLP-1R 信号传导的体外作用
进一步研究发现,GLP-1RA的促胰岛素作用与tesaglitazar的胰岛素增敏作用协同,以优化葡萄糖处理。GLP-1R介导的tesaglitazar递送将在每次单药治疗的阈下剂量下提供有益的糖代谢效应,从而在更耐受的剂量下改善全身代谢。在降低体重和改善遗传性肥胖和葡萄糖耐受不良小鼠的葡萄糖代谢方面,与GLP-1RA、tesaglitazar或GLP1RA和tesaglitazar的固定剂量组合治疗相比,GLP-1RA/tesaglitazar表现出更优异的疗效。此外,与体外结果一致,GLP-1RA/tesaglitazar 的代谢作用取决于体内功能性GLP-1R,GLP1RA/tesaglitazar 在GLP-1R敲除小鼠中不能诱导 PPARγ/RXR 异二聚化,失去了降低体重和改善葡萄糖控制的能力。
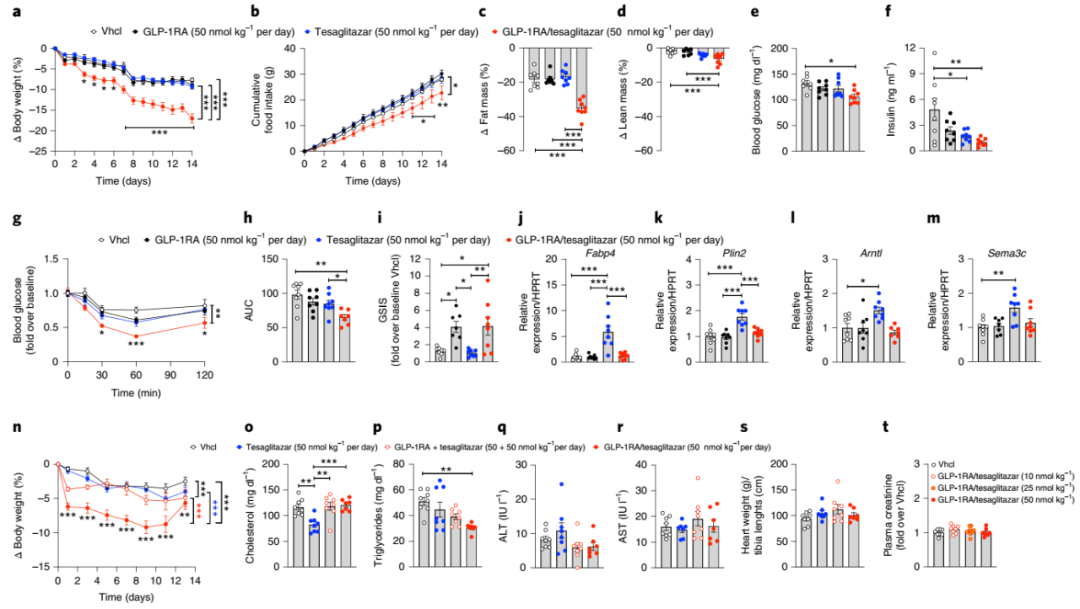 GLP-1RA/tesaglitazar 对肥胖和瘦小鼠的慢性高剂量效应
GLP-1RA/tesaglitazar 对肥胖和瘦小鼠的慢性高剂量效应
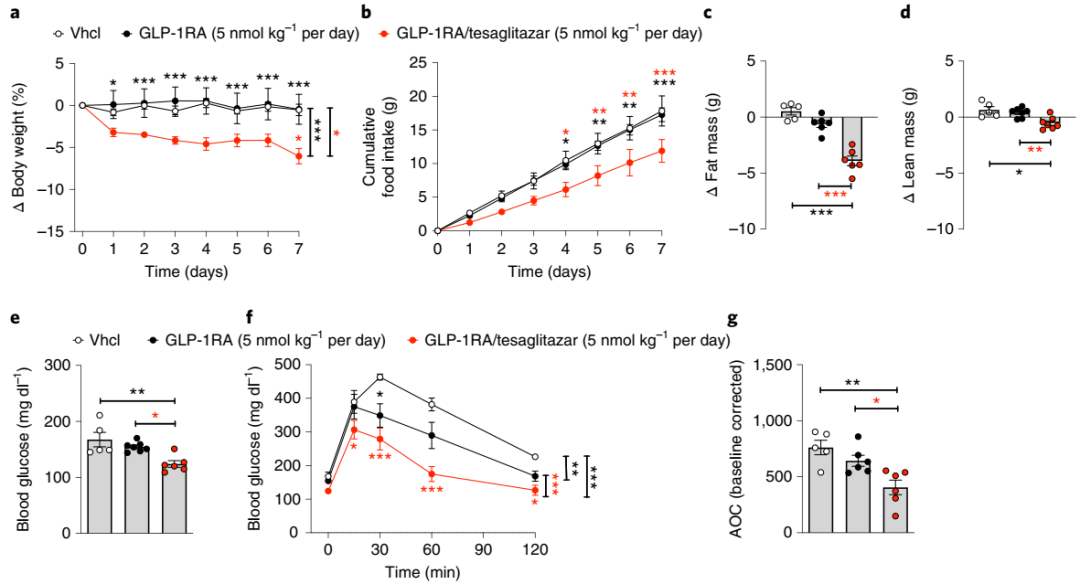
GLP-1RA/tesaglitazar 对 DIO小鼠的慢性低剂量效应
基于GLP-1RA/tesaglitazar诱导下丘脑神经元激活的能力,以及最近表明PPARγ可能通过下丘脑神经回路影响全身能量代谢的数据,研究人员最后使用液相色谱-质谱(LC-MS)的蛋白质组学鉴定了一系列新的PPAR蛋白靶标,这些靶标被tesaglitazar和GLP-1RA/tesaglitazar急性上调(而不是经过GLP-1 RA处理)。由 tesaglitazar 和 GLP-1RA/tesaglitazar 上调的丰富途径包括涉及囊泡介导的转运、神经元投射、Ca2+ 信号传导、脂质生物合成和神经递质转运的机制。GLP-1RA 和 GLP-1RA/tesaglitazar 治疗影响了几种关键激酶介导代谢信号通路(如胰岛素信号通路)的水平。这些结果表明,GLP-1RA/tesaglitazar与下丘脑中的PPAR靶点结合,下丘脑中GLP-1R的高表达允许GLP-1/tesaglitazar有利地递送到该组织中。
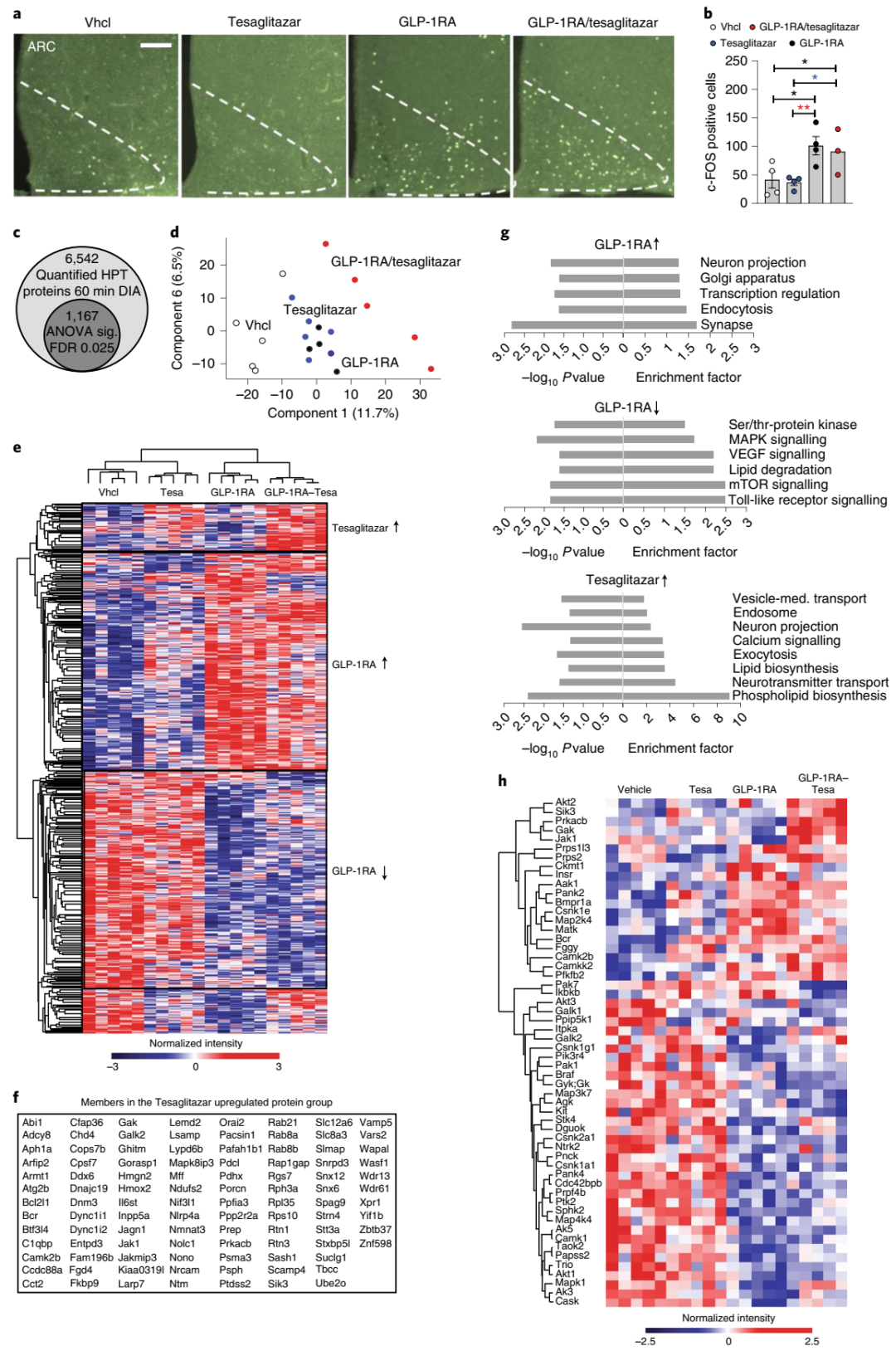 GLP-1RA/tesaglitazar 对下丘脑蛋白质组和 cFoS 的影响
GLP-1RA/tesaglitazar 对下丘脑蛋白质组和 cFoS 的影响





